- ავტორი Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:43.
- ბოლოს შეცვლილი 2025-06-01 07:37.
ალფა და ბეტა სპირალს შორის ძირითადი განსხვავება ემყარება წყალბადის კავშირის ტიპს, რომელიც მათ ქმნიან ამ სტრუქტურების შემუშავებისას. ალფა ხვეულები ქმნიან მოლეკულურ წყალბადურ კავშირებს, ხოლო ბეტა სპირალურები ქმნიან მოლეკულურ წყალბადურ კავშირებს.
კომპლექსურ ცილებს აქვთ ოთხი სტრუქტურული ორგანიზაციული დონე - პირველადი, მეორადი, მესამეული და მეოთხეული. ცილების მეორადი სტრუქტურები ქმნიან პეპტიდურ ჯაჭვებს სხვადასხვა ორიენტაციაში. პეპტიდური ჯაჭვები შედგება ამინომჟავების თანმიმდევრობებისაგან, რომლებიც დაკავშირებულია პეპტიდური ბმებით. ამრიგად, ცილებში არსებობს ორი ძირითადი მეორადი სტრუქტურა, როგორიცაა ალფა სპირალი და ბეტა სპირალი. გარდა ამისა, არსებობს სხვა მეორადი სტრუქტურები, რომლებსაც უწოდებენ ბეტა შემობრუნებას და თმის სამაგრის სტრუქტურებს.ძირითადად, ეს სტატია ყურადღებას ამახვილებს განსხვავებაზე ალფა და ბეტა სპირალს შორის.
რა არის Alpha Helix?
პროტეინებს აქვთ ორგანიზაციის ოთხი სტრუქტურული დონე. მათგან ალფა სპირალი ცილების ყველაზე გავრცელებული მეორადი სტრუქტურაა. და ეს სტრუქტურა ჩნდება როგორც ღერო, რომელიც დახვეულია ცენტრალური ღერძის გარშემო. გარდა ამისა, ალფა სპირალი არის მარჯვენა ხელის სპირალი. თუმცა, შესაძლოა არსებობდეს მარცხენა ხვეულიც. აქ პეპტიდური ბმები იქმნება ამინო-ტერმინალიდან კარბოქსი-ტერმინალამდე. ამინომჟავები უკავშირდებიან ერთმანეთს ამ პეპტიდური ობლიგაციების მეშვეობით. წყალბადის შიდა მოლეკულური ბმები არის ალფა სპირალის წარმოქმნის მთავარი მიზეზი.
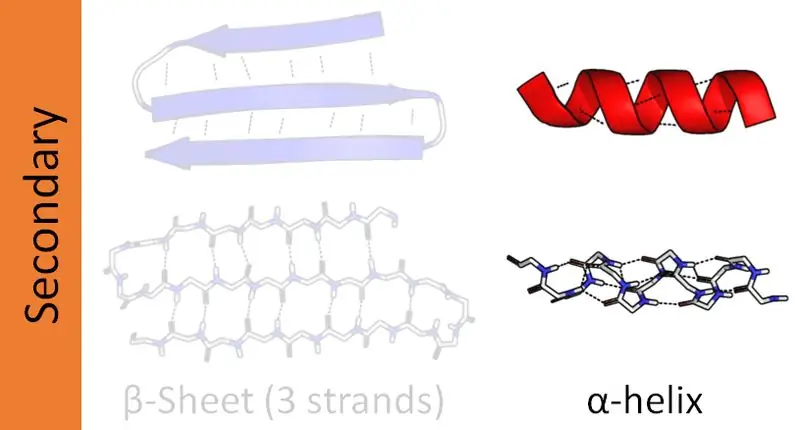
სურათი 01: Alpha Helix
ალფა სპირალის განლაგება დამოკიდებულია ცილის ჰიდროფილურ და ჰიდროფობიურ ბუნებაზე.თუ ამინომჟავების თანმიმდევრობა შედგება ჰიდროფილური R (ცვლადი) ჯგუფების დიდი რაოდენობით, R ჯგუფები ორიენტირებულია წყლის ფაზაზე. თუ ცვლადი ჯგუფები ჰიდროფობიურია, ისინი გამოდიან გარემოს ჰიდროფობიურ ფაზაში. ორივე სცენარში, R ჯგუფები, როგორც ჩანს, ვრცელდება ხვეული სტრუქტურიდან. ამ სტრუქტურული მახასიათებლების გამო, ალფა სპირალი უფრო მდგრადია მუტაციების მიმართ. ამრიგად, წყალბადის ობლიგაციების არსებობა ასტაბილურებს ალფა სპირალის სტრუქტურას. ალფა სპირალში საშუალოდ არის 3,6 ნარჩენი თითო ბრუნვაში, რადგან წყალბადის ბმების განვითარებას სჭირდება 3,6 ნარჩენი. ზოგიერთი სტრუქტურული ცილა, როგორიცაა კოლაგენი და კერატინი, მდიდარია ალფა სპირალებით.
რა არის Beta Helix?
ბეტა სპირალი ცილის მეორე ყველაზე გავრცელებული მეორადი სტრუქტურაა. მიუხედავად იმისა, რომ ის არც ისე გავრცელებულია, როგორც ალფა სპირალი, ბეტა სპირალის არსებობა ასევე მნიშვნელოვან როლს ასრულებს ცილის სტრუქტურაში. ბეტა სპირალის ფორმირება ხდება ორი ბეტა ფურცლის მეშვეობით, რომლებიც მოწყობილია ან პარალელურად ან ანტიპარალელურად.ეს ფურცლები შემდეგ ყალიბდება ხვეული სტრუქტურაში. მოლეკულათაშორისი წყალბადური ბმები ორ ფურცელ ძაფს შორის ხელს უწყობს ბეტა სპირალის წარმოქმნას.

სურათი 02: ბეტა ჰელიქსი
ბეტა ხვეულები შეიძლება იყოს როგორც მემარჯვენე, ასევე მარცხენა ხელით, მათი შეკვრის შაბლონებიდან გამომდინარე. ბეტა სპირალის ფორმირებისას, ორი ბეტა ფურცლის ცვლადი ჯგუფები განლაგდება სპირალის ბირთვში. ამიტომ, ბეტა ფურცლების შემქმნელი ჯგუფების უმრავლესობას აქვს ჰიდროფობიური ფუნქციები.
ალფა სპირალისგან განსხვავებით, 17 ნარჩენი ქმნის ერთ ბრუნს ბეტა სპირალებში. ლითონის იონებს აქვთ ბეტა სპირალის წარმოქმნის გააქტიურების უნარი. ალფა სპირალის მსგავსად, წყალბადის ბმები მხარს უჭერენ ბეტა სპირალის სტრუქტურის შენარჩუნებას. კარბოანჰიდრაზას ფერმენტი და პექტატ ლიაზა ორი ცილაა, რომელიც მდიდარია ბეტა სპირალებით.
რა მსგავსებაა ალფა და ბეტა ჰელიქსს შორის?
- ალფა და ბეტა ჰელიქსი არის ცილების ორი მეორადი სტრუქტურა.
- ამინომჟავები ორივე მეორადი სტრუქტურის მონომერია.
- გარდა ამისა, ალფა და ბეტა სპირალის ქიმიური შემადგენელი კომპონენტებია ნახშირბადი, წყალბადი, ჟანგბადი, აზოტი და გოგირდი.
- ასევე, ორივე მეორადი სტრუქტურა გადაიქცევა უფრო მაღალი დონის ორგანიზაციად.
- უფრო მეტიც, ორივე სტაბილიზირებულია წყალბადის ბმებით.
- ორივე სტრუქტურაში ჰიდროფობიურობა განისაზღვრება ამინომჟავების R ჯგუფების არსებობით.
რა განსხვავებაა ალფა და ბეტა ჰელიქსს შორის?
ალფა და ბეტა სპირალს შორის მთავარი განსხვავებაა წყალბადის კავშირის ტიპი, რომელსაც ისინი აჩვენებენ. ალფა სპირალი აჩვენებს მოლეკულურ წყალბადურ კავშირს, ხოლო ბეტა სპირალი აჩვენებს მოლეკულურ წყალბადურ კავშირს.გარდა ამისა, ალფა სპირალი ქმნის მარჯვენა სპირალს, ხოლო ბეტა სპირალს შეუძლია შექმნას როგორც მარჯვენა, ასევე მარცხენა სპირალი. ასე რომ, ეს ასევე მნიშვნელოვანი განსხვავებაა ალფა და ბეტა სპირალს შორის.
უფრო მეტიც, კიდევ ერთი განსხვავება ალფა და ბეტა სპირალს შორის არის ის, რომ ალფა სპირალის ფორმირება ხდება ამინომჟავების თანმიმდევრობის გადახვევით, ხოლო ბეტა სპირალის წარმოქმნისას ორი ბეტა ფურცელი ან პარალელური ან ანტიპარალელური უკავშირდება. შექმენით ხვეული სტრუქტურა.
ქვემოთ მოცემული ინფოგრაფიკა წარმოგიდგენთ მეტ ინფორმაციას ალფა და ბეტა სპირალს შორის სხვაობის შესახებ.

რეზიუმე - ალფა vs ბეტა ჰელიქსი
როგორც ალფა სპირალი, ასევე ბეტა სპირალი მნიშვნელოვანია პროტეინის რთული სტრუქტურების იდენტიფიკაციისა და დედუქციისთვის. ორივე ტიპი არის ცილების მეორადი სტრუქტურები.თუმცა, ალფა სპირალი არის ამინომჟავების თანმიმდევრობების ხვეული ტრიალი. ამის საპირისპიროდ, ბეტა სპირალის ფორმირება ხდება პარალელური ან ანტიპარალელური ბეტა ფურცლების წყალბადური კავშირის საშუალებით. გარდა ამისა, წყალბადის კავშირი არის ინტრამოლეკულური ალფა სპირალის სახით, ხოლო წყალბადის კავშირი არის ინტერმოლეკულური ბეტა სპირალის სახით. გარდა ამისა, ორივე ამ სტრუქტურას აქვს R ჯგუფი, რომელიც განსაზღვრავს ცილის ჰიდროფობიურობას. ამრიგად, ეს აჯამებს განსხვავებას ალფა და ბეტა სპირალს შორის.






